科伦药业5月16日公告,其子公司科伦博泰,于2022年5月13日与MSD签署许可协议修正案,将其具有自主知识产权的生物大分子肿瘤项目A,有偿独家许可给默沙东(MSD)进行中国以外区域范围内的商业化开发。

根据协议,默沙东将根据商业化开发阶段向科伦博泰支付首付款、各类里程碑付款及相应净销售额提成。科伦博泰于许可协议生效时收到1700万美元一次性、不可退还的付款,于本协议修正案签署后收到3000万美元一次性、不可退还的付款,里程碑付款累计不超过13.63亿美元,并按双方约定的净销售额比例提成。

值得注意的是,科伦药业并未公开本次授权的具体药物,而是语焉不详地以“具有自主知识产权的生物大分子肿瘤项目”指代。外界推测,本次授权的药物,大概率是科伦药业具有自主知识产权TROP2-ADC,代号SKB264。
TROP2作为一个新兴的泛瘤种靶点,在三阴乳腺癌、非小细胞肺癌、卵巢癌等多个瘤种中高表达。SKB264通过TROP2单抗将连接的新型毒素分子更直接的靶向到肿瘤细胞,能够有效降低药物的脱靶毒性,同时兼顾疗效和安全性。
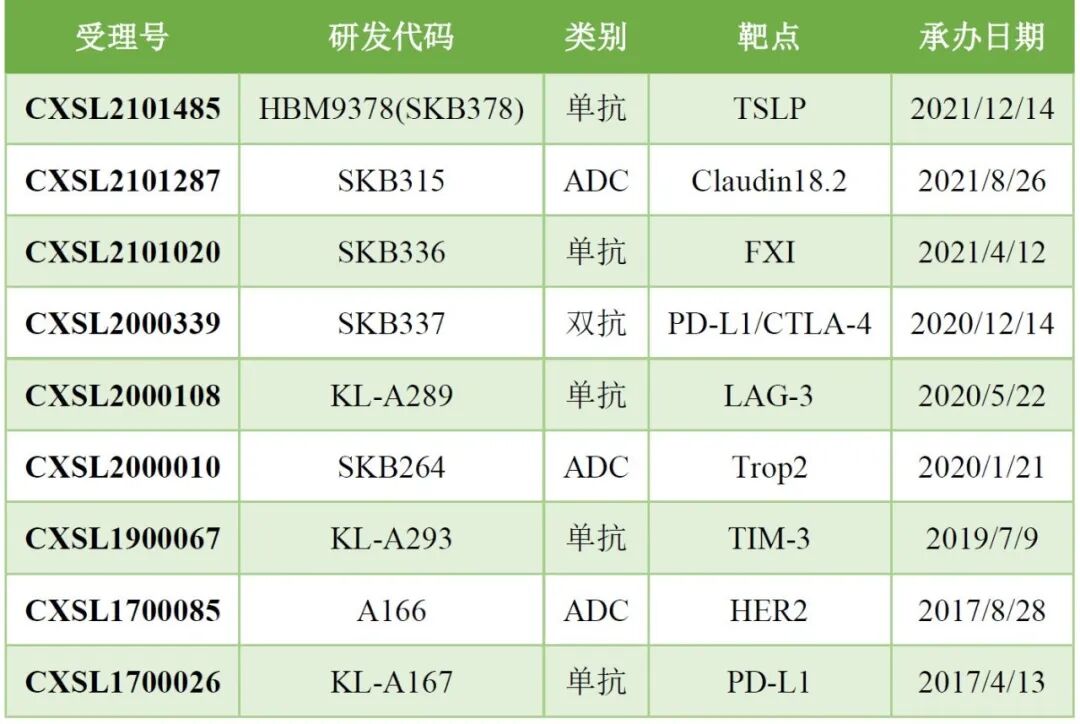
科伦药业大分子新药研发管线,图源医药笔记
2021年欧洲肿瘤内科学会(ESMO)年会,来自MD Anderson的 Jordi Rodon Ahnert教授,以口头报告形式公布了SKB264(TROP2-ADC)国际多中心Ⅰ期临床研究结果。
SKB264的这项在局部晚期或转移性实体瘤患者中的开放、国际多中心研究,由Jordi Rodon Ahnert教授和同济大学附属东方医院李进教授共同担任主要研究者。
入组人群均为经过多线治疗失败的、局部晚期或转移性实体瘤患者。截至2021年3月15日,中美共入组18例患者至2、4和6 mg/kg 3个剂量组,55.6%的患者既往接受过≥4个治疗方案。17例患者接受至少1次疗效评估,总缓解率(ORR)为35.3%(6/17),疾病控制率(DCR)为70.6%(12/17)。
目前,SKB264正在中美开展针对多个瘤种的II期临床试验,已初步获得了令人期待的临床数据,同时也在积极推进联合用药的临床研究。
近期,SKB264联合PD-L1单抗KL-A167加或不加铂类治疗的II期临床试验,获得CDE批准开展,将为不限PD-L1表达的晚期或转移性非小细胞肺癌(NSCLC)患者,提供可能的全新治疗手段。
值得注意的是,全球范围已经有TROP2-ADC药物上市。吉利德的Trodelvy是目前全球唯一一款获批上市的靶向Trop2的ADC药物,适应症包括三阴乳腺癌(TNBC)和局部晚期或转移性尿路上皮癌(UC)。除此之外,阿斯利康/第一三共的DS-1062也该领域很有竞争力的产品。
近年来,国产创新药越来越受到国际大药企的认可,中国也逐步成为生物医药领域技术和产品输出的重要基地,交易标的也更加多元,已从早期的PD-1扩展到更多差异化产品。期待中国创新药能早日走上国际舞台,造福全球患者。